Os cientistas observaram que as células mieloides no hipotálamo protegem contra os efeitos de dietas hipercalóricas
Com mais de 600 milhões de pessoas afetadas pela obesidade no mundo e projeções que indicam que esse número ultrapassará 1 bilhão até 2030 (World Obesity), pesquisadores da Universidade de Campinas, orientados pelo Dr. Licio Velloso, vice-coordenador do INCT em neuroimunomodulação, deram um importante passo na compreensão dos mecanismos biológicos da doença ao identificar como células mieloides, originárias na medula óssea, recrutadas para o hipotálamo desempenham um papel fundamental na proteção contra os efeitos nocivos de dietas ricas em gordura (HFD- sigla em inglês para High-Fat Diet). O estudo revelou que essas células, especialmente as que expressam o receptor de quimiocinas CXCR3, podem oferecer novas estratégias terapêuticas para combater a obesidade e suas complicações metabólicas.
O estudo intitulado “CXCR3-expressing myeloid cells recruited to the hypothalamus protect against diet-induced body mass gain and metabolic dysfunction” faz parte da temática pesquisada pela professora Natália Mendes. A autora, durante seu pós-doutorado no Centro de Pesquisa em Obesidade e Comorbidades (OCRC) da Universidade Estadual de Campinas (UNICAMP) concentrou seus estudos na programação metabólica fetal de células imunes no hipotálamo, investigando como a dieta hiperlipídica influencia a infiltração de células imunes no hipotálamo e seu impacto no metabolismo energético e glicêmico; e no envolvimento de quimiocinas na disfunção endotelial e neurogênese hipotalâmica”, estudando o papel das quimiocinas nos processos de disfunção endotelial e neurogênese adulta no hipotálamo em modelos experimentais de obesidade.
Durante as investigações, os pesquisadores observaram a hipótese de que a ativação de células mieloides específicas e sua migração para o hipotálamo podem ser um mecanismo protetor contra a inflamação hipotalâmica, que é frequentemente associada à obesidade e resistência à insulina. O hipotálamo é uma região do cérebro que regula funções vitais como o apetite, o gasto energético e o metabolismo. Em condições normais, ele mantém o equilíbrio entre ingestão calórica e gasto energético. No entanto, dietas ricas em gorduras podem desencadear uma inflamação que prejudica sua função. Os pesquisadores notaram , através de ressonância magnética em adultos e crianças com obesidade, glioses hipotalâmicas, fornecendo evidências clínicas para a existência de uma inflamação hipotalâmica associada à obesidade.
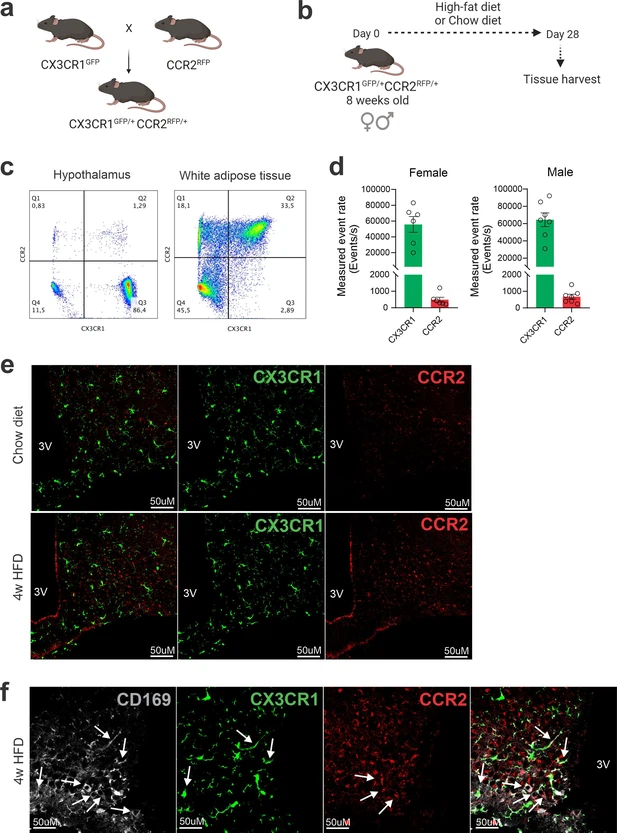
Com o uso de camundongos geneticamente modificados, os cientistas analisaram as diferenças entre as microglias residentes, células imunes do sistema nervoso central, e as células mieloides recrutadas durante o consumo de uma HFD. Eles descobriram que, enquanto as microglias residentes apresentaram alterações mínimas em seus perfis transcricionais, as células mieloides recrutadas mostraram mudanças significativas, indicando sua participação ativa na resposta inflamatória. Entre essas células recrutadas, aquelas que expressam o receptor CXCR3 se destacaram por desempenhar um papel protetor, ajudando a mitigar os efeitos metabólicos negativos da dieta rica em gordura. Quando CXCR3 foi inibido, os camundongos apresentaram aumento de peso corporal (adiposidade), glicemia elevada e alterações na expressão de genes hipotalâmicos envolvidos no controle energético e inflamação.
O estudo também revelou diferenças marcantes entre os animais machos e fêmeas na resposta das células mieloides recrutadas, com implicações significativas para o desenvolvimento de tratamentos personalizados. O dimorfismo sexual, provavelmente influenciado por hormônios, mostrou que fêmeas apresentam respostas metabólicas distintas em relação aos machos, reforçando a necessidade de considerar o sexo nos futuros estudos e tratamentos relacionados à obesidade.
Estudos anteriores na área mostraram que gorduras dietéticas, particularmente ácidos graxos saturados de cadeia longa, desencadeiam uma resposta inflamatória no hipotálamo mediobasal que surge poucas horas após a introdução de uma HFD e progride para um estado crônico com o consumo prolongado da dieta. As microglias desempenham um papel central nessa resposta inflamatória, e estudos demonstraram que, durante o consumo prolongado de HFD, ocorre o recrutamento de células derivadas da medula óssea, que passam a compor uma nova paisagem de microglias hipotalâmicas.
As descobertas atuais abrem caminho para o desenvolvimento de novas terapias direcionadas ao receptor CXCR3 e seus ligantes, como CXCL10, que podem reduzir a inflamação hipotalâmica sem os efeitos adversos associados às abordagens imunossupressoras convencionais. Além disso, a pesquisa destacou o papel distinto das células mieloides recrutadas em comparação às microglias residentes, sugerindo que cada tipo celular tem funções únicas na inflamação hipotalâmica.
Este estudo representa um avanço significativo na busca por soluções que combatam a obesidade ao mesmo tempo que oferece uma perspectiva mais ampla sobre a plasticidade celular e as respostas inflamatórias no cérebro. Ele, não apenas aprofunda o entendimento dos mecanismos subjacentes à obesidade, mas também oferece novas possibilidades para tratamentos mais eficazes.
O artigo publicado na eLIFE completo pode ser encontrado através do link abaixo:







